Das „Scharfschützengewehr“ der humoralen Immunantwort
- Martin Döhring

- 2. März
- 2 Min. Lesezeit
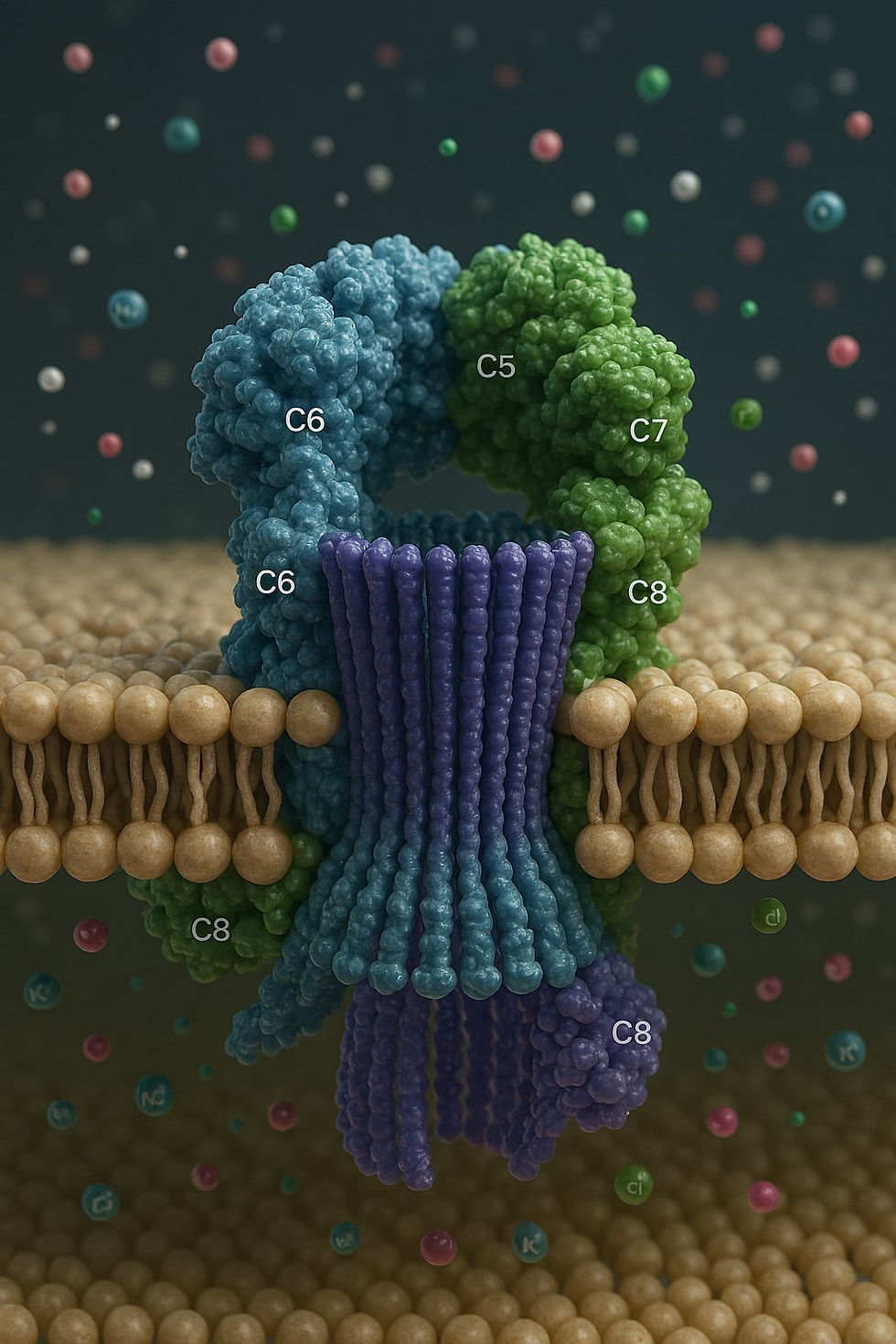
Der Membranangriffskomplex (MAC, C5b–9) – molekulare Mechanik der Zelllyse
1️⃣ Initialisierung: Die C5-Spaltung – der irreversible Kipppunkt
Unabhängig vom Eintrittspfad – klassisch (C1q/Antikörper), Lektin (MBL) oder alternativ (Tick-over) – konvergiert die Kaskade in der Bildung der C5-Konvertase:
Klassisch/Lektin: C4b2a3b
Alternativ: C3bBbC3b
?Der molekulare Schnitt:
C5 → C5a + C5b
Fragment | Funktion |
C5a | Hochpotentes Anaphylatoxin; bindet C5aR1 (CD88); induziert Chemotaxis, Degranulation, oxidative Burst |
C5b | Instabil allein; bleibt oberflächenassoziiert; dient als Keimzelle des MAC |
⚠️ Bedeutung: Mit der C5-Spaltung verlässt das System die Opsonisierungsphase und betritt die lytische Phase.
2️⃣ Assemblierung: Vom löslichen Komplex zur Membranstruktur (C5b–C8)
Die MAC-Bildung ist ein sequenzieller, strukturell hochkoordinierter Prozess:
Schritt 1: C5b + C6 → C5b6
Stabilisierung von C5b
Noch löslich
Schritt 2: + C7 → C5b67
Konformationsänderung
Exposition hydrophober Domänen
Insertion in äußere Lipidmembran
➡ Der Komplex wird membranassoziiert.
Schritt 3: + C8 → C5b678
C8 besteht aus α, β, γ
C8α penetriert die Membran tief
Bildung einer ersten instabilen Transmembranstruktur
➡ Präpore entsteht.
3️⃣ Polymerisation: Die C9-Pore – strukturelle Vollendung
Der finale Schritt ist die C9-Polymerisation.
Rekrutierung:
10–18 C9-Moleküle
Ringförmige Anlagerung um C5b-8
Strukturbiologie:
Enthält MACPF-Domäne (Membrane Attack Complex/Perforin)
Homolog zu Perforin der NK-Zellen
β-Haarnadel-Strukturen inserieren in Membran
Dimension:
Innendurchmesser ≈ 10 nm
Transmembran-β-Barrel
➡ Aus einer Undichtigkeit wird eine irreversible Nanopore
Der Todesmechanismus: Osmotische Katastrophe
Sobald die Pore stabilisiert ist:
Ionendynamik:
K⁺-Efflux
Na⁺-Influx
Ca²⁺-Dysregulation
Osmotische Konsequenz:
Wasser strömt ein
Zellvolumen steigt
Membranspannung überschreitet mechanische Stabilität
Ergebnis:
Bakterien: Mechanische Lyse
Kernhaltige Zellen: Sublytischer Stress → Ca²⁺-abhängige Signalkaskaden → Apoptose oder Nekrose
Regulierung – Schutz vor Eigenlyse
Humane Zellen exprimieren Komplementregulatoren:
Protein | Mechanismus |
CD59 (Protectin) | Blockiert C9-Polymerisation |
DAF (CD55) | Zerlegt C3/C5-Konvertasen |
MCP (CD46) | Cofaktor für Faktor I |
Fehlt CD59 (z. B. bei paroxysmaler nächtlicher Hämoglobinurie), entsteht unkontrollierte MAC-vermittelte Hämolyse.
Biophysikalische Perspektive
Die MACPF-Proteinfamilie (C9, Perforin, Gasdermine) nutzt ein konserviertes Prinzip:
Lösliche Monomere
Oligomerisierung
Konformationswechsel
β-Faltblatt-Insertion
Membranperforation
Es handelt sich um eine evolutionär konservierte pore-forming protein (PFP)-Strategie.
Funktionale Zusammenfassung
Komponente | Rolle |
C5b | Assemblierungsnukleus |
C6 | Stabilisierung |
C7 | Membranverankerung |
C8 | Initiale Penetration |
n × C9 | β-Barrel-Pore |
Klinische Relevanz (2025/2026)
Anti-C5-Therapeutika (z. B. Eculizumab, Ravulizumab) blockieren C5-Spaltung
Einsatz bei:
Paroxysmaler nächtlicher Hämoglobinurie
Atypischem HUS
Myasthenia gravis (komplementvermittelt)
Die Hemmung erfolgt upstream → keine C5b-Bildung → kein MAC.
Systemische Interpretation
Der Membranangriffskomplex ist:
Das einzige vollständig lytische Endmodul des Komplementsystems
Ein molekularer Übergang von enzymatischer Amplifikation zu physikalischer Zerstörung
Strukturell homolog zu zellulären Zytotoxizitätsmechanismen (Perforin)
✅ Präzise Ein-Satz-Zusammenfassung
Die C5-Konvertase initiiert durch Spaltung von C5 die lytische Phase des Komplementsystems, worauf C5b sequentiell C6–C9 rekrutiert, eine MACPF-vermittelte β-Barrel-Pore von ~10 nm bildet und durch unkontrollierten Ionentransport eine osmotische Lyse der Zielzelle induziert – sofern regulatorische Schutzproteine wie CD59 dies nicht verhindern.



Der Membranangriffskomplex (MAC, C5b–C9) ist die Endstufe des Komplementsystems der angeborenen Immunität. Er bildet Poren in Zellmembranen, was zur osmotischen Lyse der Zielzelle führt. Mein Gedanke, ihn gezielt gegen Tumorzellen einzusetzen, wird tatsächlich in der Tumorimmunologie und Antikörpertherapie untersucht.
Ich erkläre zuerst die molekulare Mechanik, danach die therapeutische Nutzung.
1. Molekulare Mechanik des Membranangriffskomplexes
Der MAC entsteht in mehreren aufeinanderfolgenden Schritten der Komplementkaskade.
Schritt 1 – Bildung von C5b
Die C5-Konvertase spaltet:
C5 → C5a + C5b
C5b ist ein instabiles Aktivierungsfragment, das sofort weitere Komplementproteine bindet.
Schritt 2 – Bildung des C5b-7 Komplexes
Sequenz:
C5b bindet C6
→ C5b6
C5b6 bindet C7
→ C5b-7
Eigenschaften:
C5b-7 wird hydrophob
lagert sich in die Lipidmembran der Zielzelle ein
Schritt 3 – Einbau von C8
Danach bindet: