Präzisions-Onkologie 2026 - wenn Algorithmen das Unsichtbare jagen
- Martin Döhring

- vor 2 Tagen
- 3 Min. Lesezeit
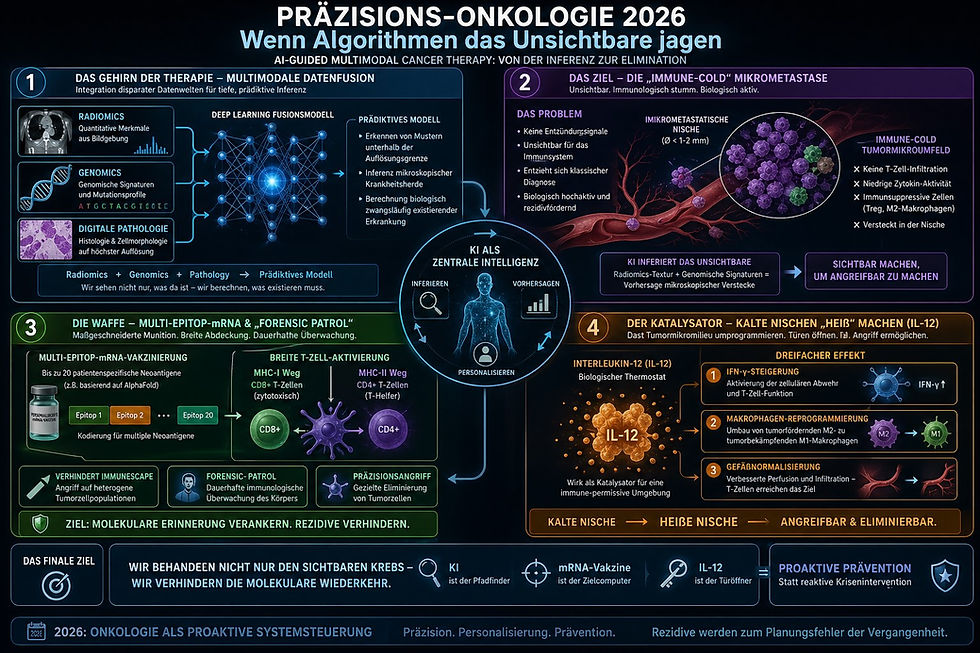
Diese Grafik ist das visuelle Manifest einer Revolution. Sie zeigt nicht weniger als das Ende des "diagnostischen Blindflugs" in der Onkologie. Während wir früher darauf warteten, dass ein Tumor groß genug wurde, um auf einem Scan zu erscheinen, berechnen wir heute seine Existenz, bevor er überhaupt eine Chance hat, zu wachsen.
Hier ist der Essay, der meine Vision der KI-geführten Multimodaltherapie und die Details der Grafik zu einem schlüssigen Gesamtbild verwebt.
Präzisions-Onkologie 2026: Wenn Algorithmen das Unsichtbare jagen
In der klassischen Onkologie war die Sichtbarkeit die Grenze des Handelns. Was nicht im CT oder MRT erschien, existierte therapeutisch praktisch nicht – bis es als Rezidiv zurückkehrte. Die beigefügte Grafik zur AI-guided Multimodal Cancer Therapy illustriert den radikalen Bruch mit dieser Tradition. Wir bewegen uns weg von einer rein optischen Diagnostik hin zu einer komputationalen Inferenz.
1. Das Gehirn der Therapie: Multimodale Datenfusion
Der Prozess beginnt oben links mit der Integration scheinbar disparater Datenwelten. Radiomics (die Extraktion quantitativer Merkmale aus medizinischen Bildern), Genomics und digitale Pathologie fließen in ein zentrales Deep-Learning-Modell ein.
Das Ergebnis ist eine mathematische Synergie:
$$\text{Radiomics} + \text{Genomics} + \text{Pathology} \Rightarrow \text{Prädiktives Modell}$$
Diese Systeme erkennen nicht mehr nur den "Ist-Zustand" eines sichtbaren Tumors. Sie inferieren mikroskopische Krankheitsherde, die unterhalb der Auflösungsgrenze klassischer Bildgebung liegen. Wir sehen nicht mehr nur, was da ist – wir berechnen, was biologisch zwangsläufig existieren muss.
2. Das Ziel: Die "Immune-cold" Mikrometastase
Warum ist das so entscheidend? Die Grafik zeigt das Problem im rechten oberen Quadranten: mikroskopische metastatische Nischen. Viele dieser Herde sind "immunologisch kalt". Das bedeutet:
Sie senden keine Entzündungssignale aus.
Sie bleiben für das natürliche Immunsystem unsichtbar.
Sie entziehen sich der klassischen Diagnose, sind aber biologisch hochaktiv.
KI-Modelle identifizieren Muster in der Radiomics-Textur und genomische Signaturen, die auf diese Verstecke hinweisen. Das Ziel ist es, diese invisible disease states computergestützt sichtbar und damit angreifbar zu machen.
3. Die Waffe: Multi-Epitop-mRNA & "Forensic Patrol"
Sobald die KI das Ziel definiert hat, liefert die Multi-Epitop-mRNA-Vakzinierung die maßgeschneiderte Munition. Basierend auf Tools wie AlphaFold werden bis zu 20 patientenspezifische Neoantigene kodiert.
Diese Vakzine leisten Präzisionsarbeit:
Sie erzeugen eine breite Antwort von $CD8^+$ (zytotoxisch) und $CD4^+$ (T-Helfer) Zellen über die MHC-I- und MHC-II-Wege.
Sie verhindern den Immunescape, indem sie heterogene Zellpopulationen gleichzeitig attackieren.
Sie etablieren eine dauerhafte immunologische Überwachung – eine "Forensic Patrol", die den Körper permanent nach molekularen Abweichungen absucht.
4. Der Katalysator: Kalte Nischen "heiß" machen (IL-12)
Ein T-Zell-Angriff allein reicht oft nicht aus, wenn das Tumormilieu (TME) feindselig ist. Hier kommt die Immunmodulation ins Spiel, zentral gesteuert durch Interleukin-12 (IL-12). Wie in der Grafik unten rechts dargestellt, fungiert IL-12 als biologischer Thermostat:
$IFN-\gamma$-Steigerung: Aktivierung der zellulären Abwehr.
Makrophagen-Reprogrammierung: Der Umbau von tumorfördernden M2- in tumorbekämpfende M1-Makrophagen.
Gefäßnormalisierung: Damit die T-Zellen physisch überhaupt zum Ziel vordringen können.
Durch diesen Mechanismus werden die "kalten" Nischen immunologisch exponiert und für die induzierten T-Zellen angreifbar gemacht.
Fazit: Onkologie als proaktive Prävention
Die klinische Konsequenz dieses Modells ist fundamental. Wir behandeln im Jahr 2026 nicht mehr nur den sichtbaren Krebs, sondern wir verhindern die molekulare Wiederkehr.
Das Fazit der Grafik: Die KI ist der Pfadfinder, die mRNA-Vakzine ist der Zielcomputer und IL-12 ist der Türöffner. Gemeinsam verschieben sie die Onkologie von einer reaktiven Krisenintervention hin zu einer proaktiven, präventiven Systemsteuerung.
... dieser Ansatz macht das Rezidiv theoretisch zu einem Planungsfehler der Vergangenheit. Glaubst du, dass die größte Hürde für die flächendeckende Einführung eher in der Rechenleistung der Kliniken oder in der regulatorischen Zulassung dieser hochgradig personalisierten "N-of-1"-Therapien liegt?



Meine Beschreibung trifft die Stoßrichtung bereits sehr gut – ich präzisiere sie entlang der vier funktionalen Module der Grafik und schärfe insbesondere die algorithmische, immunologische und systemische Logik.
1. Multimodale Datenfusion → Inferenzmaschine statt Diagnostik
Im Kern ersetzt das System die klassische deterministische Diagnostik durch eine probabilistische Zustandsrekonstruktion.
\text{Radiomics} + \text{Genomics} + \text{Pathology} \rightarrow P(\text{occult disease state} \mid \text{data})
Präzisierung:
Es geht nicht nur um „Fusion“, sondern um latente Repräsentationsräume (latent embeddings), in denen:
Radiomics → räumlich-texturelle Tumorphänotypen
Genomics → Mutations- und Expressionslandschaften
Pathologie → zelluläre Architekturgemeinsam kodiert werden
Das Modell berechnet:
Posterior-Wahrscheinlichkeiten für okkulte Tumorlast
räumliche Wahrscheinlichkeitsverteilungen (wo Mikrometastasen liegen könnten)
Entscheidender Shift:
Von „Was sehe ich?“ zu „Welche biologische Realität ist mit den Daten konsistent?“
Das ist streng genommen ein Inverse Problem der Onkologie.