Die molekulare Architektur der Lymphom-Therapie: Ein synchronisierter Angriff
- Martin Döhring

- vor 3 Tagen
- 2 Min. Lesezeit

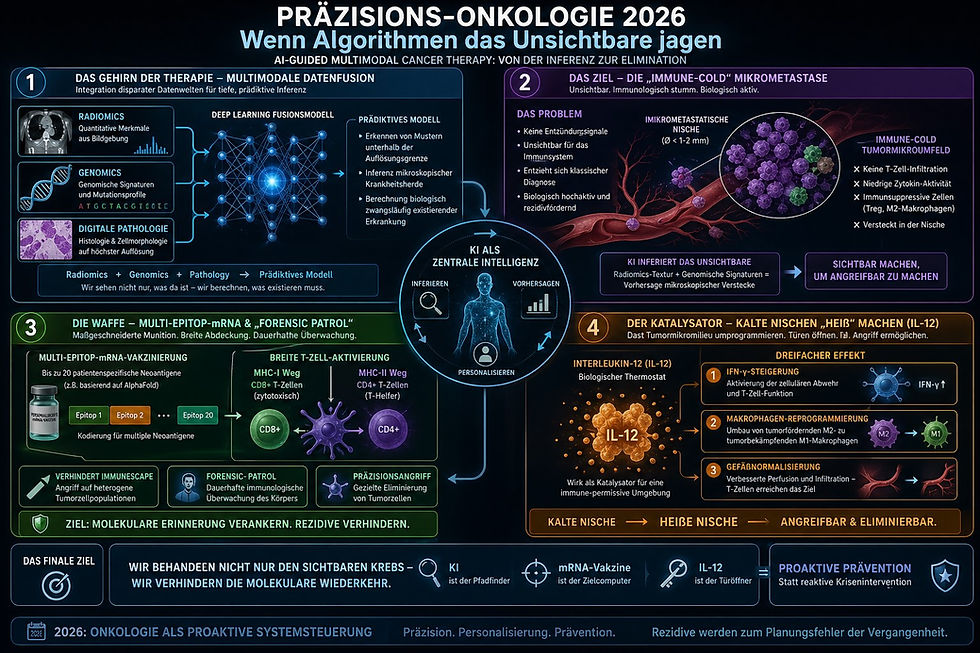
In der modernen Hämatoonkologie des Jahres 2026 hat sich das Bild des malignen Lymphoms gewandelt: Weg von einer monolithischen Erkrankung, hin zu einem komplexen, dynamischen Ökosystem. Die beigefügte Grafik verdeutlicht eindrucksvoll, dass wir den Krebs heute auf drei Ebenen gleichzeitig bekämpfen: an der Oberfläche, in der intrazellulären Signalverarbeitung und innerhalb der genetischen Software.
1. Die Belagerung der Oberfläche: Antikörper und lebende Wirkstoffe
Der erste Schlag erfolgt extrazellulär. Wie die Grafik zeigt, bilden zielgerichtete Antikörper (wie Rituximab oder Obinutuzumab) das Fundament, indem sie Oberflächenmarker wie CD20 markieren und so das körpereigene Immunsystem (ADCC/CDC) zur Exekution rufen.
Die Evolution dieses Ansatzes sind die Antibody-Drug-Conjugates (ADCs) – quasi molekulare Trojanische Pferde. Sie nutzen die Spezifität des Antikörpers, um eine hochtoxische Ladung (Cytotoxic Payload) direkt in der Lymphomzelle abzuliefern, während gesundes Gewebe weitgehend geschont wird. Die Krönung dieser Entwicklung stellt die CAR-T-Zell-Therapie dar: Hier werden T-Zellen zu lebenden Medikamenten umprogrammiert, die mittels chimärer Antigenrezeptoren (CAR) Jagd auf CD19- oder CD20-positive Zellen machen und eine massive Zytokin-Antwort auslösen.
2. Sabotage der inneren Maschinerie: Small Molecule Inhibitors
Wenn die Zelle die Belagerung an der Oberfläche übersteht, greifen „Kleine Moleküle“ (Small Molecules) in das Getriebe der Signalwege ein. Die Grafik illustriert hier zentrale Knotenpunkte:
BTK-Inhibitoren (Ibrutinib, Acalabrutinib): Sie unterbrechen den B-Zell-Rezeptor-Signalweg, die Lebensader vieler NHL-Subtypen.
BCL-2-Inhibitoren (Venetoclax): Sie blockieren den „Überlebens-Schild“ der Zelle und zwingen sie zurück in die Apoptose (den programmierten Zelltod).
PI3K-Inhibitoren (Copanlisib): Sie untergraben die Proliferationssignale direkt im Kern des Geschehens.
3. Das Betriebssystem hacken: Epigenetik und Immun-Checkpoints
Ein besonders faszinierender Aspekt der Grafik ist die epigenetische Therapie. Anstatt das Genom zu zerstören, wird es umprogrammiert. EZH2-Inhibitoren wie Tazemetostat greifen in das Chromatin-Remodeling ein, um fälschlicherweise stummgeschaltete Tumorsuppressorgene wieder zu reaktivieren (Gene Re-expression).
Gleichzeitig adressiert die Immuntherapie die „Erschöpfung“ der körpereigenen Abwehr. Checkpoint-Inhibitoren lösen die Bremsen (PD-1/PD-L1-Achse), während bispezifische T-Zell-Engager (BiTEs) eine physische Brücke zwischen der Tumorzelle und der T-Zelle schlagen, um eine präzise synaptische Aktivierung zu erzwingen.
4. Das Wettrüsten: Resistenzmechanismen
Die Grafik verschweigt jedoch nicht die Achillesferse dieser Hochtechnologie: den Widerstand. Maligne Lymphome sind Meister der Adaption. Durch Antigenverlust (die Zelle lässt CD19 einfach „verschwinden“) oder Bypass-Mutationen im Signalweg entziehen sie sich dem therapeutischen Zugriff. Die klonale Evolution sorgt dafür, dass unter dem Selektionsdruck der Therapie immer neue, resistentere Subklone entstehen.
Fazit: Onkologie 2026 – Von der Therapie zur KI-gestützten Präzision
Wie bereits treffend formuliert, liegt die Zukunft in der KI-gesteuerten Stratifikation. Wir behandeln nicht mehr „das Lymphom“, sondern wir nutzen AI-Modelle, um aus der Fülle molekularer Daten (NGS, Epigenomik) die perfekte Kombination aus Inhibitoren, Antikörpern und Immunmodulatoren zu orchestrieren.

1. Grundstruktur: Maligne Lymphome
Hodgkin-Lymphom (HL)
Non-Hodgkin-Lymphome (NHL)
v. a. B‑Zell-Lymphome (DLBCL, FL, MCL, CLL/SLL etc.)
T-/NK-Zell-Lymphome Frontiers
Die molekularen Therapieansätze richten sich nach Oberflächenantigenen, Signalwegen, Apoptose-Regulation, Epigenetik und Mikroumgebung.
2. Antikörper- und Antikörper-Drug-Konjugate
a) CD20‑gerichtete Antikörper (B‑Zell-Lymphome)
Rituximab, Obinutuzumab
Mechanismus: CDC, ADCC, direkte Apoptoseinduktion.
Standard in R‑CHOP, R‑Bendamustin etc. Nature
b) CD30‑gerichtet
Brentuximab Vedotin (ADC) bei klassischem HL, CD30⁺ T‑NHL.
Liefert ein Zytostatikum (MMAE) direkt in CD30⁺ Zellen. Nature
c) Weitere ADCs
Polatuzumab Vedotin (CD79b, DLBCL)
Ziel: B‑Zell-Rezeptor-nahe Strukturen, chemotherapeutische Nutzlast. pmc.ncbi.nlm.nih.gov oncoscience.us
3. Kleine Moleküle (Signalwege & Apoptose)
a) BTK‑Inhibitoren (BCR-Signaling)
Ibrutinib, Acalabrutinib, Zanubrutinib
Indikationen: MCL, CLL, Waldenström u. a.
Mechanismus: Blockade des B‑Zell-Rezeptor-Signalwegs (BTK). Nature oncoscience.us
b) PI3K‑Inhibitoren
Idelalisib, Copanlisib
Hemmen PI3K‑Isoformen in B‑Zellen, beeinflussen Überleben/Proliferation. pmc.ncbi.nlm.nih.gov pmc.ncbi.nlm.nih.gov
c) BCL‑2‑Inhibitoren
Venetoclax
Besonders relevant bei CLL, teils DLBCL/FL…