Molekulare Onkologie
- Martin Döhring

- 17. Sept. 2025
- 3 Min. Lesezeit

Definition: Die Molekulare Onkologie ist ein Teilgebiet der Krebsforschung, das die molekularen und zellulären Mechanismen untersucht, die der Entstehung, dem Wachstum und der Ausbreitung von Krebs zugrunde liegen. Der Fokus liegt auf genetischen Veränderungen, fehlerhaften Signalwegen und der Interaktion zwischen Tumor und Mikroumgebung.
---1. Grundprinzip: Vom gesunden Gewebe zum TumorKrebs ist eine genetische Erkrankung der Somazellen. Sie entsteht durch die Akkumulation von Mutationen in Schlüsselgenen, die die normale Zellkontrolle umgehen. Diese Mutationen können vererbt oder (häufiger) erworben sein (durch Umwelteinflüsse, zufällige Fehler bei der Zellteilung).
2. Die "Hallmarks of Cancer" – Die Kennzeichen des Krebses
Dieses einflussreiche Konzept von Hanahan und Weinberg beschreibt die funktionellen Fähigkeiten, die sich eine Zelle aneignen muss, um bösartig zu werden. Die molekulare Onkologie untersucht die treibenden Mechanismen dahinter.
Kennzeichen Molekulare Grundlage
1. Selbsterhaltung des Wachstumssignals Mutationen in Wachstumsfaktor-Rezeptoren (z.B. EGFR), oder downstream Komponenten (z.B. RAS, RAF). Die Zelle wächst unabhängig von externen Signalen.2. Umgehung von Wachstumshemmern Inaktivierung von Tumorsuppressorgenen (z.B. RB1, p53), die normalerweise die Zellteilung stoppen oder Apoptose einleiten.3. Resistenz gegen Zelltod (Apoptose) Verlust von pro-apoptotischen Signalen (z.B. Bax) oder Überexpression von anti-apoptotischen Proteinen (z.B. BCL-2).4. Unbegrenztes Replikationspotenzial Aktivierung der Telomerase, die die Chromosomenenden (Telomere) stabilisiert und die Zelle unsterblich macht.5. Induktion von Angiogenese Tumore produzieren Wachstumsfaktoren (z.B. VEGF), um die Bildung neuer Blutgefäße zur Nährstoffversorgung zu stimulieren.6. Aktivierung von Invasion & Metastasierung Veränderungen in Adhäsionsmolekülen (z.B. E-Cadherin-Verlust) und Aktivierung von Proteasen, die die Extrazellulärmatrix abbauen.Weitere neuere Kennzeichen7. Reprogrammierung des Energiestoffwechsels Umstellung auf Glykolyse auch bei Sauerstoffverfügbarkeit (Warburg-Effekt).8. Umgehung der Immunüberwachung Tumore entwickeln Mechanismen, um der Erkennung und Zerstörung durch das Immunsystem zu entgehen (z.B. über PD-L1 Expression).9. Genomische Instabilität & Mutation Defekte in DNA-Reparaturgenen (z.B. BRCA1/2) beschleunigen die Akkumulation von Mutationen.10. Tumorfördernde Entzündung Entzündungszellen in der Mikroumgebung unterstützen das Tumorwachstum und die Metastasierung.```mermaidflowchart TDA[Krebszelle]subgraph B[Treibende Mutationen]direction LR B1[Onkogene<br>z.B. EGFR, RAS<br>→ „Gaspedal klemmt“] B2[Tumorsuppressorgene<br>z.B. p53, RB1<br>→ „Bremse versagt“] B3[DNA-Reparaturgene<br>z.B. BRCA1/2<br>→ „Instabiles Genom“]endB --> C[Führt zu funktionellen Veränderungen]subgraph D[Die 10 Kennzeichen von Krebs] D1[Wachstumssignale<br>selbstständig] D2[Wachstumshemmer<br>umgehen] D3[Resistenz gegen<br>Zelltod] D4[Unendliche<br>Teilungen] D5[Angiogenese<br>aktivieren] D6[Invasion &<br>Metastasierung] D7[Stoffwechsel<br>umpragen] D8[Immunantwort<br>umgehen] D9[Genom-Instabilität<br>& Mutation] D10[Tumorfördernde<br>Entzündung]endC --> D```
---3. Schlüsselgene in der Molekularen Onkologie
Gen-Kategorie Funktion Beispiele & Konsequenz bei MutationOnkogene Förderung des Zellwachstums („Gaspedal“). EGFR, HER2/neu, BRAF, ALK, MYC, RAS-Familie. • Konsequenz: Dauerhaft aktiviert → unkontrolliertes Wachstumssignal.Tumorsuppressorgene Bremsen des Zellwachstums, DNA-Reparatur, Einleitung der Apoptose („Bremse“). p53, RB1, PTEN, APC, BRCA1, BRCA2. • Konsequenz: Funktionsverlust → Kontrollmechanismen fallen aus.DNA-Reparaturgene Erkennung und Reparatur von DNA-Schäden. BRCA1, BRCA2, MSH2, MLH1 (Mismatch-Reparatur). • Konsequenz: Defekt → hohe Mutationsrate (TMB-H), genomische Instabilität.
---4. Methoden der Molekularen Onkologie (Diagnostik)
Diese Techniken ermöglichen eine präzise Diagnose und Therapieauswahl ("Präzisionsonkologie").· Next-Generation Sequencing (NGS): Parallele Sequenzierung vieler Gene gleichzeitig. Erkennt Mutationen, Insertionen/Deletionen, Kopienzahländerungen, Genfusionen. · Panel-Sequenzierung: Gezielte Suche in 50-500 krebsrelevanten Genen. · Whole-Exome/Genome-Sequenzierung: Umfassende Analyse aller Gene bzw. des gesamten Genoms.· Immunhistochemie (IHC): Visualisierung spezifischer Protein-Expression im Tumorgewebe (z.B. HER2, PD-L1, Hormonrezeptoren).· Fluoreszenz-in-situ-Hybridisierung (FISH): Nachweis von Genvervielfältigungen (Amplifikationen, z.B. HER2) oder Genfusionen (z.B. ALK).· PCR-basierte Methoden: Hochempfindlicher Nachweis spezifischer Mutationen oder Mikrosatelliteninstabilität (MSI).
---5. Translation in die Therapie: Gezielte Therapien & Immuntherapie
Das Verständnis molekularer Mechanismen führt zu zielgerichteten Behandlungen.
Therapieprinzip Molekularer Target
Beispiele
Kleine Moleküle (small molecules) Hemmen spezifische, aktivierte Onkoproteine innerhalb der Zelle. EGFR-Inhibitoren (Osimertinib), BRAF-Inhibitoren (Dabrafenib), ALK-Inhibitoren (Crizotinib).Therapeutische Antikörper Binden extrazelluläre Domänen von Rezeptoren oder Liganden. Trastuzumab (anti-HER2), Cetuximab (anti-EGFR), Bevacizumab (anti-VEGF).Immuncheckpoint-Inhibitoren Blockieren die "Bremsen" des Immunsystems (T-Zellen). PD-1/PD-L1 Inhibitoren (Pembrolizumab), CTLA-4 Inhibitoren (Ipilimumab). Wirken besonders gut bei hoher Mutationslast (TMB-H) oder MSI-H.PARP-Inhibitoren Nutzen den Defekt in DNA-Reparaturwegen aus ("synthetische Letalität"). Olaparib bei Tumoren mit BRCA1/2-Mutationen oder anderen HRD-Defekten.
---6. Klinische Bedeutung & Zukunftsperspektiven·
Präzisionsonkologie: Die Therapieentscheidung richtet sich nicht primär nach dem Tumortyp (z.B. Lungenkrebs), sondern nach den molekularen Treibermechanismen (z.B. EGFR-Mutation).· Liquid Biopsy ("Flüssigbiopsie"): Analyse von zellfreier Tumor-DNA (ctDNA) aus dem Blut. Ermöglicht nicht-invasive Verlaufskontrolle, Detection von Resistenzen und Früherkennung von Rezidiven.· Minimal Residual Disease (MRD): Hochempfindlicher Nachweis kleinster Mengen an verbliebenen Tumorzellen nach Therapie, um das Rückfallrisiko einzuschätzen.· Neue Horizonte: CAR-T-Zelltherapien, Krebsimpfungen (insb. auf Neoantigen-Basis), Targeting von Splicing-Varianten und der Tumormikroumgebung.
Zusammenfassung: Die Molekulare Onkologie hat die Krebsbehandlung revolutioniert. Sie verschiebt den Fokus von der Anatomie des Tumors hin zu seinem molekularen Profil und ermöglicht so immer gezieltere, personalisierte und effektivere Therapien für Patienten.


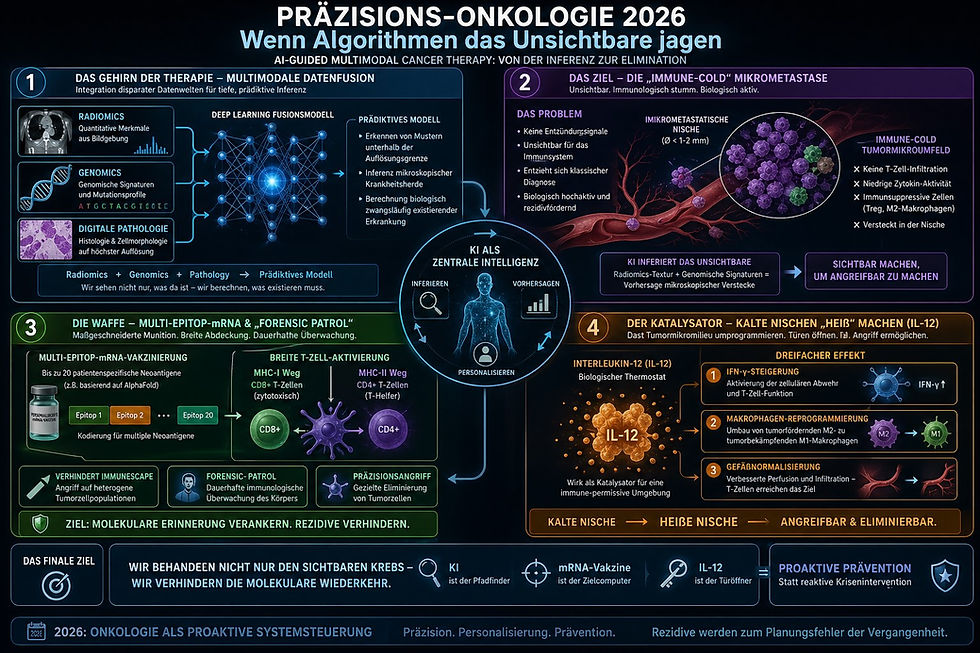
Mit modernen molekularbiologischen Verfahren wird Krebs nicht mehr primär unspezifisch bekämpft, sondern gezielt auf Ebene von Genen, Signalwegen und Zelloberflächen adressiert. Im Folgenden eine präzise Einordnung.
1. Vom unspezifischen Angriff zur gezielten Therapie
Klassische Krebstherapien (Chemotherapie, Bestrahlung) wirken vor allem auf schnell teilende Zellen. Das erklärt sowohl ihre Wirksamkeit als auch ihre erheblichen Nebenwirkungen.
Neue molekularbiologische Techniken verfolgen einen anderen Ansatz:
Krebszellen werden aufgrund spezifischer biologischer Merkmale erkannt,
gesunde Zellen werden möglichst geschont.
Grundlage ist die Erkenntnis, dass Krebs keine einheitliche Krankheit, sondern eine Vielzahl genetisch und molekular unterschiedlicher Erkrankungen ist.
2. Zentrale molekularbiologische Ansätze
a) Zielgerichtete („targeted“) Therapien
Hier werden definierte molekulare Strukturen angegriffen, etwa:
mutierte Rezeptoren (z. B. EGFR),
dauerhaft aktivierte Signalproteine (z. B. BRAF, ALK),
Tumor-spezifische Enzyme.
Tumorsuppressorgene — ausführlich erklärt
Kurzversion: Tumorsuppressorgene (TSG) sind Gene, die Zellen vor unkontrolliertem Wachstum, Genom-Schäden und Tumorentstehung schützen. Ihre Funktionsverluste (durch Mutationen, Deletionen, Epigenetik etc.) sind eine zentrale Ursache für Krebs. Im Gegensatz zu Onkogenen — die durch Aktivierung krebsfördernd wirken — führen bei TSG meist Verluste der Genfunktion zur Tumorentwicklung.
1) Grundfunktionen von Tumorsuppressorgenen
TSG wirken auf mehreren Ebenen:
Zellzykluskontrolle (z. B. RB-Pathway) — verhindern, dass die Zelle unkontrolliert in S-Phase eintritt.
DNA-Reparatur & Genomintegrität (z. B. BRCA1/2, MMR-Gene) — erkennen und reparieren Schäden; Verlust → erhöhte Mutationsrate.
Apoptose / Seneszenz (z. B. TP53) — bei irreparablen Schäden wird programmiert abgestorben oder dauerhaft stillgelegt.
Regulation der Zell-Zell/Matrix-Interaktion und Mikroumgebung (z. B. APC, VHL) — beeinflussen Differenzierung, Migration, Angiogenese.
Genomstabilität / Chromatin-Remodelling (z. B. ARID1A) — verhindern…