Apoptose - Antikörper treiben Krebszellen in den Zelltod
- Martin Döhring

- 12. Sept. 2025
- 2 Min. Lesezeit
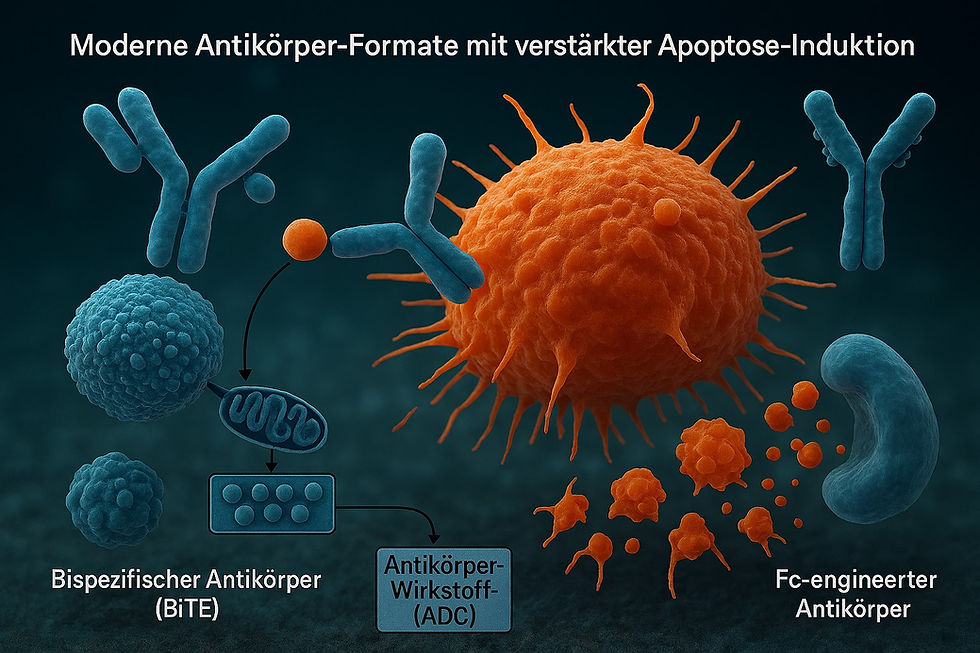
Schauen wir uns das Schritt für Schritt auf molekularer Ebene an: Es gibt mehrere Konzepte, wie Antikörper gezielt Apoptose in Krebszellen auslösen können.
1. Direkte Bindung an Todesrezeptoren (death receptor signaling)
Einige Antikörper sind gegen Todesrezeptoren der TNF-Rezeptor-Superfamilie gerichtet, z. B. TRAIL-R1 (DR4) oder TRAIL-R2 (DR5).
Diese Rezeptoren sitzen auf der Oberfläche von Tumorzellen.
Wenn ein Antikörper sie kreuzvernetzt, werden sie aktiviert → DISC (death-inducing signaling complex) bildet sich.
DISC rekrutiert FADD (Fas-associated death domain protein) und Pro-Caspase-8.
Caspase-8 wird aktiviert → aktiviert Caspase-3 → Zelle geht in Apoptose.
2. Indirekte Auslösung über Wachstumsrezeptoren
Viele therapeutische Antikörper (z. B. Trastuzumab gegen HER2, Cetuximab gegen EGFR) blockieren Wachstumsfaktor-Rezeptoren.
Normalerweise liefern diese Rezeptoren Survival-Signale (PI3K/AKT, MAPK).
Antikörper hemmen diese Signale → das Gleichgewicht kippt Richtung Pro-Apoptose.
Gleichzeitig können Tumorzellen dadurch empfindlicher gegenüber Chemotherapie oder Immuneffektorzellen werden.
3. Antikörper-abhängige zelluläre Zytotoxizität (ADCC)
Therapeutische Antikörper binden an ein Tumorantigen (z. B. CD20 bei Lymphomen → Rituximab).
Ihr Fc-Teil wird von Fcγ-Rezeptoren auf NK-Zellen, Makrophagen oder Granulozyten erkannt.
NK-Zellen setzen Perforin und Granzym B frei.
Perforin bildet Poren.
Granzyme aktivieren Caspase-3 direkt oder über die mitochondriale Achse (Bid → Bax/Bak → Cytochrom c).
Das resultiert in Apoptose der Tumorzelle.
4. Komplementaktivierung (CDC)
Manche Antikörper aktivieren Komplement (klassischer Weg → C1q bindet Fc).
Endprodukt ist MAC (membrane attack complex) → kann Zellen direkt zerstören.
Zusätzlich fördert Komplement die Phagozytose und verstärkt apoptotische Signalwege.
5. Mitochondrialer Weg (intrinsische Apoptose)
Indirekt: Durch Blockade von Survival-Signalen oder durch crosslinking bestimmter Oberflächenantigene (z. B. CD20 durch Rituximab).
Es kommt zur Aktivierung von Bax/Bak → Mitochondrien setzen Cytochrom c frei.
Cytochrom c + Apaf-1 + dATP → Apoptosom → Caspase-9 → Caspase-3 → Apoptose.
🔑 Kurz gesagt: Antikörper können Tumorzellen über mehrere Ebenen in die Apoptose treiben:
direkt durch Aktivierung von Todesrezeptoren,
indirekt durch Blockade von Überlebenssignalen,
durch Immunzellen (ADCC) oder Komplement,
und über mitochondriale Kaskaden.


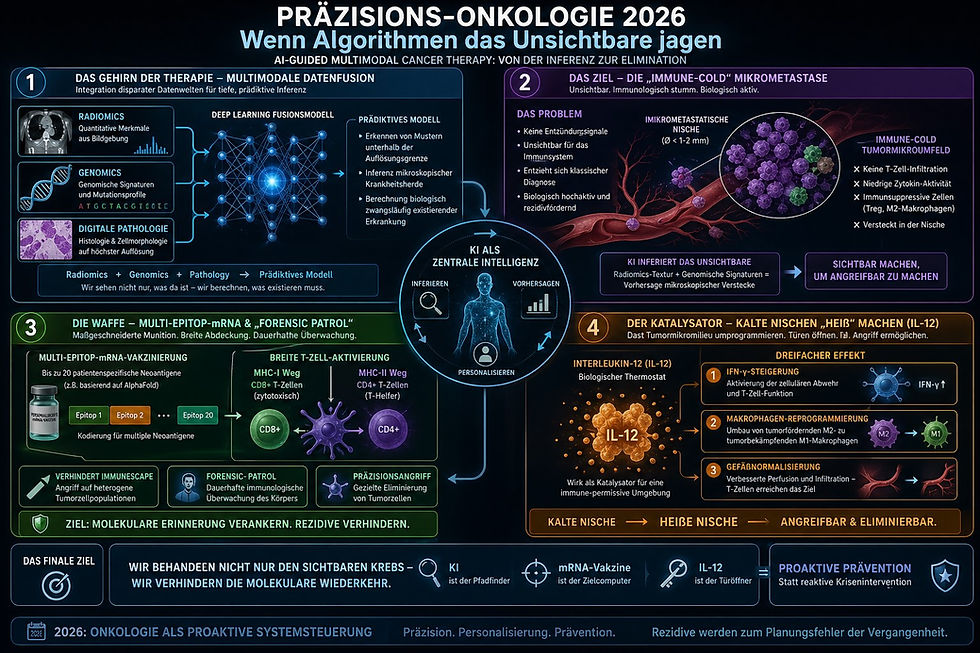

Wenn ein Tumor stirbt – etwa durch Chemotherapie, Strahlentherapie oder Immunaktivierung – können bestimmte Laborparameter im peripheren Blutbild Hinweise auf diesen Zerfallsprozess geben. Diese Werte sind nicht spezifisch, aber sie zeigen molekulare und immunologische Reaktionen an.
🧪 Relevante Laborparameter bei Tumorzerfall
Laborwert
Bedeutung beim Tumorsterben
Typischer Befund
LDH (Laktatdehydrogenase) Zellzerfall → Freisetzung aus Tumorzellen
Erhöht
CRP (C-reaktives Protein) Entzündungsreaktion durch Nekrose oder Immunantwort
Erhöht Leukozytenzahl
Immunantwort oder Knochenmarkstress
Erhöht oder erniedrigt Harnsäure
DNA-Abbau → Purinfreisetzung
Erhöht (Tumorlyse-Syndrom) Kalium, Phosphat, Kalzium
Elektrolytverschiebung bei massivem Zellsterben
Kalium ↑, Phosphat ↑, Kalzium ↓ D-Dimere / Fibrinogen
Gerinnungsaktivierung bei Tumornekrose
D-Dimere ↑, Fibrinogen ↓ Ferritin
Akute-Phase-Protein, auch bei Tumornekrose erhöht
Erhöht Transaminasen (ALT/AST)Leberbeteiligung oder systemische Nekrose Erhöht
🔥 Spezialfall: Tumorlyse-Syndrom
Bei sehr schnellem Tumorzerfall…
1. Direkte Bindung an Todesrezeptoren (Death Receptor Signaling)
Deine Beschreibung ist präzise: Antikörper gegen TRAIL-Rezeptoren (z. B. DR4/DR5) oder Fas (CD95) können durch Crosslinking die extrinsische Apoptose-Kaskade initiieren. Der DISC-Komplex mit FADD und Pro-Caspase-8 führt tatsächlich zu Caspase-8-Aktivierung, die dann Effektorkaspasen wie Caspase-3 aktiviert. Ergänzung: In klinischen Ansätzen werden agonistische Antikörper entwickelt, die speziell diese Rezeptoren auf Tumorzellen aktivieren, ohne gesunde Zellen zu stark zu beeinträchtigen – ein Beispiel ist Mapatumumab (gegen DR4).
2. Indirekte Auslösung über Wachstumsrezeptoren
Richtig, Antikörper wie Trastuzumab (Herceptin) oder Cetuximab blockieren Rezeptortyrosinkinasen (z. B. HER2 oder EGFR), was zu einer Unterdrückung pro-survival Pathways wie PI3K/AKT und MAPK führt. Das verschiebt das Gleichgewicht hin zu pro-apoptotischen Signalen, oft verstärkt durch Kombinationstherapien. Zusätzlich können diese Antikörper Zellzyklusarrest…